LA TABLA PERIÓDICA DE LOS ELEMENTOS
2. SÍMBOLOS QUÍMICOS
2.1. ORGANIZACIÓN DE LOS ELEMENTOS
UN POCO DE HISTORIA...
A continuación te presentamos una cronología de algunas propuestas de clasificación de los elementos químicos:
¿CÓMO ES LA TABLA PERIÓDICA ACTUAL?...
Es importante que a partir de ahora tengan una tabla periódica disponible; de esa manera podrán ir siguiendo de manera práctica la lectura del material que se presenta a continuación.
La tabla periódica que se utiliza actualmente está relacionada con la estructura electrónica de los átomos. En ella se encuentran todos los elementos conocidos, tanto los 92 que se hallaron en la Naturaleza como los que se obtuvieron en el laboratorio por medio de reacciones nucleares.
Las principales características de la tabla periódica son:
-
- Los elementos están ordenados por su número atómico creciente (Z). Comienza por el 1H, sigue con el 2He, 3Li, 4Be, 5B, etc.
-
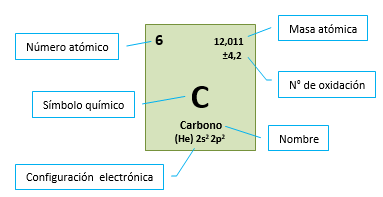
A cada elemento le corresponde un casillero donde figura su símbolo y otros datos, tales como el número atómico, el número másico, la configuración electrónica, etc.
-
- Las filas horizontales se denominan períodos y las columnas verticales son conocidas como grupos o familias.
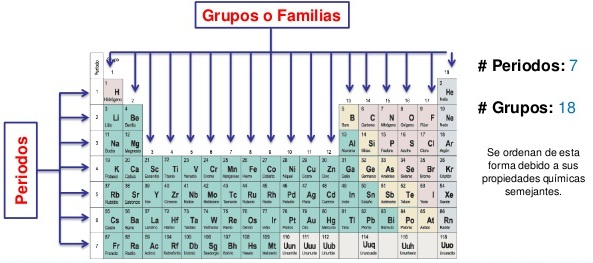
FUENTE: IMAGEN OBTENIDA DE TABLAS PERIÓDICAS PERIODOS Y GRUPOS - Bing images
-
- En total la tabla tiene 7 periodos que están numerados de manera creciente de arriba hacia abajo, desde 1 a 7.
- Las propiedades de los elementos de un período cambian de manera progresiva al recorrer la tabla.
- Cada grupo (columnas verticales) contiene una familia de elementos que tienen propiedades similares.
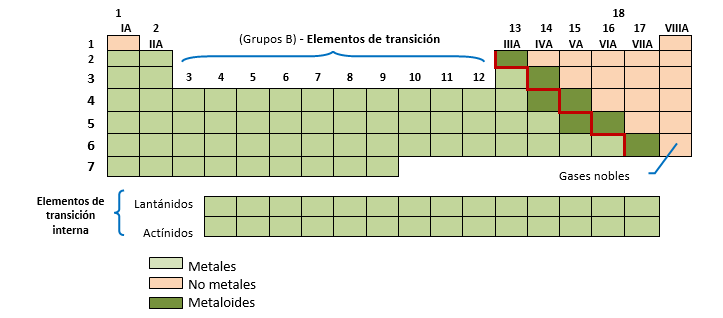
Coexisten dos maneras de referirse a los grupos: una de ellas los numera de 1 a 18 y van a través de toda la tabla, de izquierda a derecha. La otra utiliza números romanos del I al VIII, subdividiendo la tabla en dos tipos de grupos, los A y los B. Los grupos A se denominan representativos, mientras que con la letra B se designa a los elementos que ocupan el bloque central de la tabla periódica llamados elementos de transición.
Existe otro grupo de 28 elementos conocidos con el nombre de elementos de transición interna. Éstos por comodidad se ubican aparte pero corresponden al 6° y 7° período de la tabla. También son conocidos como Lantánidos y Actínidos.
Muchos grupos de la tabla periódica reciben nombres especiales: el grupo 1 o IA, metales alcalinos (Li, Na, K, etc.); los del grupo 17 o VIIA son los halógenos (F, Cl, Br, I, At) y los del grupo 18 o VIII gases nobles o inertes, denominados de esta manera por su escasa reactividad química (He, Ne, Ar, Kr, Zn, Rn).
Resumiendo, podemos definir al sistema periódico actual en los siguientes términos: Las propiedades de los elementos químicos son una función periódica (cíclica) del número atómico.
En otras palabras también podemos decir:
Fuente: El siguiente texto fue extraído del libro “QUÍMICA Aula Taller, General e Inorgánica”, José Mautino, Editorial Stella.