FORMULACIÓN Y NOMENCLATURA DE COMPUESTOS INORGÁNICOS PARTE II
4. RESUMEN DE COMPUESTOS INORGÁNICOS
El siguiente esquema resume los tipos de compuestos inorgánicos desarrollados en estas dos semanas y los reactivos involucrados en su formación.
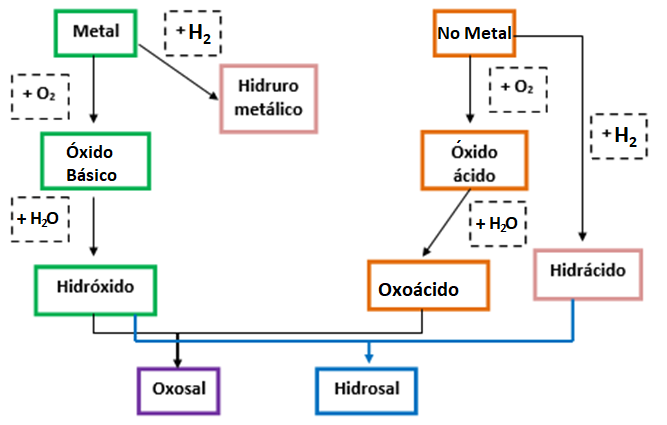
A modo de resumen se podría decir que, los metales pueden, por un lado, combinarse con H2 para dar lugar a los hidruros metálicos y por el otro, con O2 para formar óxidos básicos. Los óxidos básicos, a su vez, pueden combinarse con H2O dando lugar así a los hidróxidos.
Por otra parte, los elementos no metálicos y algunos elementos de transición (conocidos como anfóteros) pueden combinarse con O2 para formar óxidos ácidos o anhídridos. Estos, a su vez, pueden combinarse con H2O para dar formar oxoácidos. Así también, ciertos elementos no metálicos (halógenos y anfígenos) pueden combinarse con H2 para formar hidruros no metálicos, mayormente de naturaleza gaseosa, que se disuelven en agua para formar hidrácidos que se hallan en forma de solución acuosa.
Finalmente, de la reacción de un hidróxido y un hidrácido se produce una hidrosal y H2O; mientras que de la reacción entre un hidróxido y un oxoácido se obtiene una oxosal y H2O. Es importante que tengas en cuenta las reglas para asignar números de oxidación a la hora de formarlos y que recuerdes cómo varía la nomenclatura tradicional en cada caso.

