FORMULACIÓN Y NOMENCLATURA DE COMPUESTOS INORGÁNICOS PARTE I
 . . . Imagen extraída de: Cuaderno de cultura científica "De los compuestos químicos"
. . . Imagen extraída de: Cuaderno de cultura científica "De los compuestos químicos"
3. COMBINACIONES BINARIAS
3.2. Combinaciones Binarias con Oxígeno
Las combinaciones binarias con Oxígeno son comúnmente llamadas Óxidos. En general, los óxidos están formados por oxígeno y cualquiera de los restantes elementos de la tabla periódica. Excepto por el Flúor que, al ser más electronegativo que el oxígeno, en realidad forma el fluoruro de oxígeno y el Hidrógeno, ya explicado anteriormente. (Peterson, 2013).
Antes de comenzar a trabajar en los tipos de óxidos, te proponemos que realices la lectura del texto “Oxígeno” de Garrido y Bianchi, publicado en “El gato y la Caja”.
-
- Óxidos Básicos: Son compuestos binarios constituidos por un elemento metálico y Oxígeno, donde este último siempre trabaja con número de oxidación -2.
Se obtienen de acuerdo con la siguiente ecuación general:
Metal + O2 --> Óxido básico
Ejemplo: 2Fe + O2 --> 2FeO
Fórmula Química: Queda determinada por el metal y el oxígeno, cuyas valencias o números de oxidación se intercambian y se anotan como subíndices.
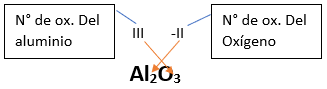
En el caso de que sean múltiplos, se simplifican; por ejemplo:
Fe2O2 --> FeO
Nomenclatura:
Según la nomenclatura tradicional:
➡️ Si el metal con el que se combina el oxígeno tiene una sola valencia, se nombra con las palabras Óxido de..., y el nombre del metal con el que se combina. Ejemplo: Al2O3; Óxido de Aluminio.
➡️Si el metal con el que se combina al oxígeno tiene dos valencias se utilizan los sufijos “oso” e “ico” y se suprime la sílaba “de”:
⏺️ “oso” cuando el elemento usa la menor valencia; Ejemplo: FeO, valencia del hierro (II): Óxido ferroso
⏺️ “ico” cuando el elemento va con la mayor valencia; Ejemplo: Fe2O3, valencia del hierro (III): Óxido férrico.
Ahora te proponemos que leas con atención el siguiente tutorial paso a paso para formular un Óxido Básico.
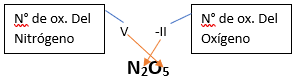
Para repasar lo que leíste, te proponemos que observes y tomes nota del siguiente video tutorial. Autor: Holzmaisters Jonathan. Te proponemos que realices una actividad sobre la formulación de los óxidos básicos. Para acceder haz CLIC AQUÍ. ______________________________________________________________________________________________________________________________ No metal + O2 --> Anhídrido Ejemplo: 2N2 + 5O2 --> 2N2O5 Fórmula Química: Queda determinada por el no metal y el oxígeno, cuyas valencias o números de oxidación se intercambian y se anotan como subíndices. En el caso de que sean múltiplos, se simplifican. Por ejemplo: S2O6 --> SO3 Nomenclatura: Según la nomenclatura tradicional: ➡️ Si el no metal con el que se combina el oxígeno tiene una sola valencia, se nombra con las palabras Anhídrido de..., y el nombre del metal con el que se combina. ➡️ Si el no metal con el que se combina al oxígeno tiene dos valencias se utilizan los sufijos “oso” e “ico” y se suprime la sílaba “de”: ⏺️ “oso” cuando el elemento usa la menor valencia; Ejemplo: N2O3, valencia del nitrógeno (III): Anhídrido nitroso. ⏺️ “ico” cuando el elemento va con la mayor valencia; Ejemplo: N2O5, valencia del nitrógeno (V): Anhídrido nítrico. ➡️ Si el no metal con el que se combina al oxígeno tiene cuatro valencias se utilizan prefijos “hipo” y “per” y los sufijos “oso” e “ico” y se suprime la sílaba “de”; por ejemplo: cloro, que posee las valencias 1, 3, 5 y 7. ⏺️ Cuando la valencia es 1, se utiliza el prefijo “hipo” y el sufijo “oso”; Anhídrido hipocloroso. ⏺️ Cuando la valencia es 3, se utiliza solamente el sufijo “oso”; Anhídrido cloroso. ⏺️ Cuando la valencia es 5, se utiliza solamente el sufijo “ico”; Anhídrido clórico. ⏺️ Cuando la valencia es 7, se utiliza el prefijo “per” y el sufijo “ico”; Anhídrido perclórico. Ahora te proponemos que leas con atención el siguiente tutorial paso a paso para formular un Óxido ácido o anhídrido. Para repasar lo que leíste, te proponemos que observes y tomes nota del siguiente video tutorial. Autor: Holzmaisters Jonathan. Te proponemos que realices una actividad sobre la formulación de los óxidos ácidos. Para acceder haz CLIC AQUÍ.
Tutorial paso a paso 4: Formación de un óxido básico a partir de su nombre
En este tutorial plantearemos la ecuación de formación de un oxido básico, con el objetivo de obtener su fórmula, usando como referencia el nombre que obtiene por nomenclatura tradicional.
Vamos paso a paso:
Paso 1: En primer lugar, debemos conocer el nombre del compuesto y a partir del mismo, y junto a las reglas de nomenclatura, extraer la información necesaria:
Paso 2: Escribimos las fórmulas de los reactivos, en este caso, oxígeno (O2) y plomo (Pb), separados por un signo + (no importa el orden de los reactivos, puede escribirse el O2 o el Pb primero y luego el otro):
Paso 3: Luego de los reactivos agregamos la flecha de reacción (-->):
Paso 4: Empezamos a platear la fórmula del óxido, para ello escribimos el símbolo del metal (Pb) seguido del símbolo del oxígeno (sin separarlos con +), después de la flecha de reacción:
Paso 5: En la tabla periódica buscamos los números de oxidación de cada elemento:
Paso 6: Teniendo en cuenta el nombre del compuesto seleccionamos el número de oxidación o valencia correspondiente para cada elemento: El O utilizará el -2 y el Pb el +2 (menor), ya que el nombre termina en “oso”.
Paso 7: Escribimos en lápiz los valores seleccionados anteriormente en números romanos sobre cada elemento (este paso es opcional):
Paso 8: Escribimos el número de oxidación del oxígeno como subíndice del plomo y viceversa, luego borramos los números de oxidación que escribimos en lápiz:
Importante: siempre que, en un compuesto todos los subíndices sean múltiplos entre sí, es necesario simplificarlos, para obtener la formula más sencilla del óxido. En este caso debemos dividir ambos subíndices por 2, quedando de la siguiente manera:
Paso 9: Revisamos si la ecuación esta balanceada, para ello debemos verificar que cada elemento aparezca la misma cantidad de veces en reactivos y en productos:
Paso 10: Finalmente, Si la ecuación no se encuentra balanceada, es preciso realizar esta operación, mediante el uso de los coeficientes estequiométricos. En este caso se debe agregar un 2 delante del PbO en productos para que coincida la cantidad de oxígeno y luego un 2 frente al Pb en reactivos para que la cantidad de plomo coincida:
Y de esta manera obtenemos la ecuación balanceada del Óxido Plumboso.
Autor: Holzmaisters Jonathan.


Tutorial paso a paso 5: Formación de un anhídrido a partir de su nombre
En este tutorial plantearemos la ecuación de formación de un anhídrido, con el objetivo de obtener su fórmula, usando como referencia el nombre que obtiene por nomenclatura tradicional.
Vamos paso a paso:
Paso 1: En primer lugar, debemos conocer el nombre del compuesto para, a partir de este y teniendo en cuenta las reglas de nomenclatura, poder extraer la información necesaria:
Paso 2: Escribimos las fórmulas de los reactivos, en este caso oxígeno (O2) y cloro (Cl2), separados por un signo + (no importa el orden de los reactivos, puede escribirse el O2 o el Cl2 primero y luego el otro):
Paso 3: Luego de los reactivos agregamos la flecha de reacción (-->):
Paso 4: Empezamos a platear la formula del anhídrido, para ello escribimos el símbolo del no metal (Cl) seguido del símbolo del oxígeno (sin separarlos con +), después de la flecha de reacción:
Paso 5: En la tabla periódica buscamos los números de oxidación de cada elemento:
Paso 6: Teniendo en cuenta el nombre del compuesto seleccionamos el número de oxidación o valencia correspondiente para cada elemento: El O utilizará el -2 y el Cl el +7 (la mayor de los 4 positivos), ya que el nombre comienza con “per” y termina en “ico”.
Paso 7: Escribimos en lápiz los valores seleccionados anteriormente en números romanos sobre cada elemento (este paso es opcional):
Paso 8: Escribimos el número de oxidación del oxígeno como subíndice del cloro y viceversa, luego borramos los números de oxidación que escribimos en lápiz:
Importante: siempre que, en un compuesto todos los subíndices sean múltiplos entre sí, es necesario simplificarlos, para obtener la formula correcta del anhídrido. En este caso los subíndices no cumplen con esta condición, por lo que se mantienen igual:
Paso 9: Revisamos si la ecuación esta balanceada, para ello debemos verificar que cada elemento aparezca la misma cantidad de veces en reactivos y en productos:
Paso 10: Finalmente, si la ecuación no se encuentra balanceada, debemos hacerlo empleando coeficientes estequiométricos. En este caso se debe agregar un 2 delante del Cl2O7 en productos y un 7 delante del O2 en los reactivos para que coincida la cantidad de oxígeno y luego se debe agregar un 2 frente al Cl2 en reactivos para que la cantidad de cloro coincida:
Y de esta manera obtenemos la ecuación balanceada del Anhídrido Perclórico.
Autor: Holzmaisters Jonathan.


Ahora que terminaste de leer este libro, te invitamos a que realices el CUESTIONARIO DEL TEMA donde encontrarás actividades relacionadas a todo lo abordado en este material. Puedes comenzar haciendo CLIC AQUÍ.